Содержание:
В кремний Это неметаллический и в то же время металлоидный элемент, обозначаемый химическим символом Si. Это полупроводник, который является неотъемлемой частью компьютеров, калькуляторов, сотовых телефонов, солнечных элементов, диодов и т.д .; это практически главный компонент, который позволил установить цифровую эпоху.
Кремний всегда присутствовал в кварце и силикатах, оба минерала составляют около 28% от массы всей земной коры. Таким образом, это второй по численности элемент на поверхности Земли, а просторы пустынь и пляжей дают представление о том, насколько он богат.

Кремний относится к 14-й группе периодической таблицы, как и углерод, расположенный под ней. Вот почему этот элемент считается четырехвалентным металлоидом; имеет четыре валентных электрона и теоретически может потерять их все с образованием катиона Si4+.
Одно свойство, которое он разделяет с углем, — это его способность связываться друг с другом; то есть их атомы ковалентно связаны, образуя молекулярные цепи. Кроме того, кремний может образовывать собственные «углеводороды», называемые силанами.
Преобладающими соединениями кремния в природе являются известные силикаты. В чистом виде он может выглядеть как монокристаллическое, поликристаллическое или аморфное твердое тело. Это относительно инертное твердое вещество, поэтому оно не представляет значительного риска.
Плюсы и минусы
Кремний наделен свойствами, полезными либо нет с утилитарной точки зрения.
Недостатки вещества:
- Энергозатратность при получении чистого материала.
- Хрупкость. Но при нагреве выше 810°С кремний обретает пластичность.
Достоинства материала:
- Доступность сырья: четверть земной коры – это кремний.
- Простота технологии извлечения вещества.
- Способность образовывать линейку соединений: диоксид, силаны, силициды, силикаты. Плюс твердые конгломераты – база для создания сотен видов стекла, керамики.
- Возможности как полупроводника широкого охвата. На электрические характеристики неметалла влияют примеси. Промышленность «эксплуатирует» этот феномен для создания полупроводников заданного типа.
Главный плюс кремния – нулевая токсичность. Она облегчает использование неметалла всеми сегментами рынка, включая медицину и фармакологию.
Ковалентный характер
Этот ковалентный характер обусловлен тем, что, как и углерод, кремний имеет четыре валентных электрона в соответствии с его электронной конфигурацией:
3 с2 3p2
Для связывания чистые 3s и 2p орбитали бесполезны. Вот почему атом создает четыре гибридных sp-орбитали3, с помощью которых он может образовывать четыре ковалентные связи Si-Si и, таким образом, заполнять октет валентности для двух атомов кремния.
Затем кристалл кремния визуализируется как трехмерная ковалентная решетка, состоящая из связанных тетраэдров.
Однако эта сетка не идеальна, поскольку в ней есть дефекты и границы зерен, которые отделяют один кристалл от другого и определяют их; а когда таких кристаллов очень мало и их много, мы говорим о поликристаллическом твердом теле, идентифицируемом по его неоднородному блеску (подобному серебряной мозаике или чешуйчатой поверхности).
Где используется
Применение кремния определяют свойства. Неметалл хрупок, поэтому непригоден в качестве «скелета» конструкций. Однако эта же характеристика позволяет идеально обрабатывать поверхность кристаллов, что ценят производители электроники.

Применение кремния

Микроконтроллер 1993 года с УФ стиранием памяти 62E40 европейской фирмы STMicroelectronics. За окошечком виден кристалл микросхемы — кремниевая подложка с выполненной на ней схемой.
Промышленность
Кроме IT-индустрии неметалл востребован традиционными сегментами промышленности.

- Металлургия. Технический кремний используется как раскислитель при выплавке чугуна, упрочнитель сплавов.
- Машино-, приборостроение. Сплавы с металлами тверды, тугоплавки. Используются как компоненты турбин, термоэлементы оборудования металлургических комбинатов.
- Электро-, радиотехника. Из неметалла-полупроводника изготавливают фотоэлементы, интегральные схемы, транзисторы, диоды, другую продукцию.
- Органический, неорганический синтез.
- Прозрачность вещества для инфракрасного спектра – главный плюс для производителей оптики.
- Стекольная промышленность. Силикаты – исходник при производстве стекла, хрусталя, керамики, фарфоро-фаянсового ассортимента.
- Песок – компонент строительных материалов (цемента, бетона).
- Почти универсален карбид (кремний + углерод). Соединение закупают металлурги, приборостроители, химпром. Твердое (7 баллов по Моосу) вещество используется как полупроводник широкого диапазона действия и абразив.
- Кремнийорганические соединения закупают производители силиконовой продукции: герметиков, смазок, других изделий.
То есть применение нашлось чистому веществу и соединениям.
Другие сферы
Фармацевты используют кремниевые продукты как базис препаратов для профилактики и лечения атеросклероза, туберкулеза, артрита.
Эстетичные разновидности неметалла – агаты, аметисты, горный хрусталь, опалы, сердолик – закупают ювелиры и собиратели минералогических коллекций.
Технология получения
Цель переработки сырья – максимально чистое вещество.
В лабораториях процедура следующая:
- Добывают силицид магния.
- Воздействуют на вещество уксусной либо соляной кислотой.
- Образовавшийся моносилан очищают (сорбентами, ректификаторами), нагревают до 1050°C.
В результате получают водород и кремний.
Для промышленников сырьем служит белый песок мелких фракций (диоксид вещества с формулой SiO2).
Кристалл кремния
Способ получения неметалла предусматривает следующие этапы:
- Прокаливание смеси сырья с магнием до образования аморфной модификации. Продукт выглядит как буроватый порошок.
- Технически чистый материал (99,9%) получают в печи при 1780°C. Из расплава диоксида вещество восстанавливают коксом.
- При необходимости изымают углерод, другие примеси.
Очищают кремний прямым хлорированием. Из полученных соединений изымают примеси, восстанавливают водородом при 910-1150°C.
Монокристалл кремния, выращенный по методу Чохральского
Новые технологии очистки предусматривают замену хлора фтором: это экологичнее и рентабельнее. Есть способы получения вещества на основе дистилляции оксида неметалла, вытравкой примесей.
Солнечные панели из монокристаллов
Характерной особенностью монокристаллических солнечных панелей является однородный цвет фотоэлементов, создающий точно такой же внешний вид у всей конструкции. Цветовая гамма определяется размерами зерен выращенного монокристалла. Выращивание кремниевых слитков осуществляется из природного кремния, после чего кристаллическая решетка материала приобретает необходимую структуру и частоту.
Монокристаллические солнечные батареи считаются наиболее эффективными и применяются на различных объектах. Они имеют свои плюсы и минусы, которые следует учитывать при выборе той или иной конструкции.

Среди положительных качеств можно отметить следующие:
- Высокая эффективность изделий, благодаря высокому качеству структуры материала. Это позволяет довести коэффициент полезного действия до 17-22%.
- Возможность уменьшения размеров солнечных панелей без потерь мощности по сравнению с другими типами батарей с такими же техническими характеристиками. Таким образом, чтобы получить электроэнергию в количестве 10 ватт, потребуется монокремниевая панель с меньшими размерами.
- Максимальный срок эксплуатации, превышающий этот показатель у других изделий. При условии соблюдения всех правил и норм, батарея прослужит не менее 25 лет.
Серьезным недостатком этих конструкций является их высокая стоимость. Для многих пользователей данный фактор имеет решающее значение при выборе изделия, несмотря на все положительные качества. Поэтому нередко выбираются более дешевые поликристаллические панели, хотя и не такие эффективные.
При незначительной загрязненности или недостаточном освещении, когда отдельные элементы перестают участвовать в процессе, наступает резкая потеря производительности всей системы. В связи с этим рекомендуется использовать инверторы, способные выровнять параметры цепи и ликвидировать последствия неравномерного освещения.
Реактивность
Кремний полностью не растворим в воде, а также в сильных кислотах или щелочах. Однако он растворяется в концентрированной смеси азотной и плавиковой кислот (HNO3-HF). Точно так же он растворяется в горячем щелочном растворе, происходит следующая химическая реакция:
Si (т) + 2NaOH (водн.) + H2O (l) => Na2да3(ас) + 2H2(грамм)
Метасиликатная соль натрия, Na2да3, также образуется при растворении кремния в расплавленном карбонате натрия:
Si (s) + Na2CO3(l) => Na2да3(l) + C (s)
При комнатной температуре он вообще не реагирует с кислородом, даже при 900 ºC, когда начинает формироваться защитный стекловидный слой SiO.2; а затем, при 1400 ºC, кремний реагирует с азотом в воздухе с образованием смеси нитридов, SiN и Si.3N4.
Кремний также реагирует при высоких температурах с металлами с образованием силицидов металлов:
2Mg (тв) + Si (тв) => Mg2Да (а)
2Cu (тв) + Si (тв) => Cu2Да (а)
При комнатной температуре реагирует взрывчато и напрямую с галогенами (слой SiO отсутствует.2 чтобы защитить вас от этого). Например, у нас есть реакция образования SiF4:
Да + 2F2(г) => SiF4(грамм)
И хотя кремний нерастворим в воде, он реагирует раскаленным докрасна с потоком пара:
Да (а) + H2O (г) => SiO2(s) + 2H2(грамм)
Кремниевые формы жизни
Группа IV Периодической таблицы элементов содержит углерод C, силициум (кремний) Si и несколько тяжелых металлов. Это значит, что степень окисления кремния равна +4. Углерод, конечно, является строительным материалом жизни, какой мы ее знаем. Но теоретики альтернативной биохимии предполагают, что населенная живыми существами планета может существовать в какой-то другой солнечной системе. У такой формы жизни кремний якобы может заменять углерод.

Многие научно-фантастические произведения рассказывают о кремниевых формах жизни — чувствительные кристаллы, живые золотые песчинки и даже существа, чьими следами являются кирпичи из кремнезема. Это интересно, но неправильно. Кремний может превратиться во множество реалистичных структур, но его химические свойства делают маловероятной возможность стать основой для инопланетных форм жизни.

Действительно, углерод и силиций имеют много общих характеристик. Валентность кремния равна четырем, это означает, что отдельные атомы образуют четыре связи с другими элементами при образовании химических соединений. И силиций, и углерод связываются с кислородом. Оба образуют длинные цепи, называемые полимерами. В простейшем случае углерод дает полимер под названием полиацеталь, пластик, используемый в синтетических волокнах и оборудовании. Кремний дает полимерные силиконы, которые используются для водонепроницаемой ткани или смазки металлических и пластиковых деталей.
Но когда углерод окисляется — или соединяется с кислородом, скажем, во время горения — он становится газообразным углекислым газом; силиций же окисляется до твердого диоксида, называемого кремнеземом. Кремний окисляется до твердого вещества. Это одна из основных причин того, почему он не может поддерживать жизнь.

Кремнезем или песок — это твердое вещество, диоксид кремния образует решетку, в которой один атом силиция окружен четырьмя атомами кислорода. Силикатные соединения, содержащие SiO4−4, также существуют в ряде минералов — полевых шпатах, слюде, цеолитах, тальке. И эти твердые системы создают проблемы в том, что касается утилизации энергии для живой системы.
Жизненная форма нуждается в некотором способе сбора, хранения и использования энергии. Она должна исходить из окружающей среды. После поглощения энергия должна высвобождаться именно там, где это необходимо, и в то время, когда это нужно. В противном случае вся она может высвобождать тепло одновременно, сжигая жизненную форму.
Поликристаллический кремний
В отличие от других синтезов или производств, получение поликристаллического кремния начинается с газовой фазы силана, SiH4. Этот газ подвергается пиролизу при температуре выше 500 ºC, так что происходит термическое разложение и, таким образом, из его исходных паров поликристаллы кремния осаждаются на поверхности полупроводника.
Следующее химическое уравнение иллюстрирует протекающую реакцию:
Да H4(g) => Si (s) + H2(грамм)
Очевидно, что в камере не должно быть кислорода, так как он будет реагировать с SiH.4:
Да H4(г) + 2O2(г) => SiO2(s) + 2H2O (г)
И реакция горения такова, что она происходит быстро при комнатной температуре с минимальным воздействием воздуха на силан.
Другой синтетический путь для производства этого типа кремния начинается с кристаллического кремния в качестве сырья. Они заставляют его реагировать с хлористым водородом при температуре около 300 ºC, в результате чего образуется трихлорсилан:
Si (т.) + 3HCl (г) => SiCl3H (г) + H2(грамм)
И SiCl3H реагирует при 1100 ° C, чтобы регенерировать кремний, но теперь поликристаллический:
4SiCl3H (г) => Si (т) + 3SiCl4(г) + 2Н2(грамм)
Просто посмотрите на уравнения, чтобы получить представление о работе и строгих производственных параметрах, которые необходимо учитывать.
Где найти и получить
Кремний является седьмым по распространенности элементом во Вселенной и вторым в земной коре, а также обогащает мантию Земли своим обширным семейством минералов. Этот элемент очень хорошо связывается с кислородом, образуя широкий спектр оксидов; среди них кремнезем, SO2, силикаты (разнообразного химического состава).
Кремнезем можно увидеть невооруженным глазом в пустынях и на пляжах, поскольку песок в основном состоит из SiO.2. В свою очередь, этот оксид может проявляться в нескольких полиморфах, наиболее распространенными из которых являются: кварц, аметист, агат, кристобалит, триполи, коэсит, стишовит и тридимит. Кроме того, его можно найти в аморфных твердых телах, таких как опалы и диатомовая земля.
Между тем силикаты еще богаче структурно и химически. Некоторые силикатные минералы включают: асбест (белый, коричневый и голубоватый), полевой шпат, глины, слюды, оливины, алюмосиликаты, цеолиты, амфиболы и пироксены.
Практически все породы состоят из кремния и кислорода с их стабильными связями Si-O, а также их кремнеземов и силикатов, смешанных с оксидами металлов и неорганическими частицами.
Силиконовые полимеры
Знаменитый силиконовый клей состоит из органического полимера, поддерживаемого стабильностью цепей Si-O-Si связей … Если эти цепи очень длинные, короткие или сшитые, свойства силиконового полимера изменяются, а также их конечное применение. .
Среди его применений, перечисленных ниже, можно упомянуть следующее:
-Клей или клей, не только для соединения бумаги, но и строительных блоков, резины, стеклянных панелей, камней и т. Д.
-Смазочные материалы в гидравлических тормозных системах
-Укрепляет краски и улучшает яркость и интенсивность их цветов, позволяя им выдерживать перепады температур, не растрескиваясь и не разъедая
-Они используются в качестве водоотталкивающих спреев, благодаря которым некоторые поверхности или предметы остаются сухими.
-Они придают средствам личной гигиены (зубные пасты, шампуни, гели, кремы для бритья и т. Д.) Ощущение шелковистости
-Его покрытия защищают электронные компоненты чувствительных устройств, таких как микропроцессоры, от тепла и влажности.
— Из силиконовых полимеров сделано несколько резиновых мячей, которые подпрыгивают при падении на пол.
Физические характеристики кристаллического кремния
Элементы для солнечных панелей изготавливаются из полупроводниковых материалов. Среди них несомненным лидером является кремний, который служит основным материалом для производства панелей.
По своим физическим свойствам кремний бывает монокристаллический, поликристаллический, мультикристаллический и аморфный. Такое разнообразие структур дает ему несомненное преимущество перед другими видами полупроводников, и делает незаменимым в производстве микроэлектроники и электронной техники. То же самое в полной мере касается и солнечной энергетики. Кремний относится к наиболее распространенным химическим элементом, а его запасы практически неограниченны. Данный материал отличается доступностью, дешевизной и экологической чистотой. В природе он известен как двуокись кремния, а в натуральном виде представлен речным и кварцевым песком, кремнем, кварцем и кварцитами. Кристаллическая решетка кремния похожа на алмазную, поэтому он очень хрупкий и приобретает пластичность лишь при температуре свыше 800 градусов.
Кремний относится к наиболее распространенным химическим элементом, а его запасы практически неограниченны. Данный материал отличается доступностью, дешевизной и экологической чистотой. В природе он известен как двуокись кремния, а в натуральном виде представлен речным и кварцевым песком, кремнем, кварцем и кварцитами. Кристаллическая решетка кремния похожа на алмазную, поэтому он очень хрупкий и приобретает пластичность лишь при температуре свыше 800 градусов.
При идеальной кристаллической структуре и отсутствии примесей, в температурных условиях абсолютного нуля, кремний можно рассматривать как изолятор. При повышении температуры в нем возникает явление так называемой собственной проводимости. В этом случае электрический ток возникает за счет свободных электронов или дырок, представляющих электронную или дырочную проводимость.
Помещенный в комнатную температуру, чистый кремний ведет себя как химически инертное вещество. Однако, если температура повышается, он начинает вступать в активную реакцию с другими элементами. Особую активность данный материал проявляет в расплавленном виде, создавая серьезные проблемы при его очистке до требуемого уровня.
Солнечные элементы на основе кремния изготавливаются из тонких кремниевых пластинок, нарезаемых на установленную толщину. Предварительно они подвергаются различным видам обработки, и в результате сложных технологических процессов получается нужный материал.
СТРУКТУРА
 Кристаллическая решётка кремния кубическая гранецентрированная типа алмаза, параметр а = 0,54307 нм (при высоких давлениях получены и другие полиморфные модификации кремния), но из-за большей длины связи между атомами Si—Si по сравнению с длиной связи С—С твёрдость кремния значительно меньше, чем алмаза. Имеет объемную структуру. Ядра атомов вместе с электронами на внутренних оболочках обладают положительным зарядом 4, который уравновешивается отрицательными зарядами четырех электронов на внешней оболочке. Вместе с электронами соседних атомов они образуют ковалентные связи на кристаллической решетке. Таким образом, на внешней оболочке находятся четыре своих электрона и четыре электрона, заимствованные у четырех соседних атомов. При температуре абсолютного нуля все электроны внешних оболочек участвуют в ковалентных связях. При этом кремний является идеальными изолятором, так как не имеет свободных электронов, создающих проводимость.
Кристаллическая решётка кремния кубическая гранецентрированная типа алмаза, параметр а = 0,54307 нм (при высоких давлениях получены и другие полиморфные модификации кремния), но из-за большей длины связи между атомами Si—Si по сравнению с длиной связи С—С твёрдость кремния значительно меньше, чем алмаза. Имеет объемную структуру. Ядра атомов вместе с электронами на внутренних оболочках обладают положительным зарядом 4, который уравновешивается отрицательными зарядами четырех электронов на внешней оболочке. Вместе с электронами соседних атомов они образуют ковалентные связи на кристаллической решетке. Таким образом, на внешней оболочке находятся четыре своих электрона и четыре электрона, заимствованные у четырех соседних атомов. При температуре абсолютного нуля все электроны внешних оболочек участвуют в ковалентных связях. При этом кремний является идеальными изолятором, так как не имеет свободных электронов, создающих проводимость.
Технология получения
Цель переработки сырья – максимально чистое вещество.
В лабораториях процедура следующая:
- Добывают силицид магния.
- Воздействуют на вещество уксусной либо соляной кислотой.
- Образовавшийся моносилан очищают (сорбентами, ректификаторами), нагревают до 1050°C.
В результате получают водород и кремний.
Для промышленников сырьем служит белый песок мелких фракций (диоксид вещества с формулой SiO2).
Кристалл кремния
Способ получения неметалла предусматривает следующие этапы:
- Прокаливание смеси сырья с магнием до образования аморфной модификации. Продукт выглядит как буроватый порошок.
- Технически чистый материал (99,9%) получают в печи при 1780°C. Из расплава диоксида вещество восстанавливают коксом.
- При необходимости изымают углерод, другие примеси.
Очищают кремний прямым хлорированием. Из полученных соединений изымают примеси, восстанавливают водородом при 910-1150°C.
Монокристалл кремния, выращенный по методу Чохральского
Новые технологии очистки предусматривают замену хлора фтором: это экологичнее и рентабельнее. Есть способы получения вещества на основе дистилляции оксида неметалла, вытравкой примесей.
ПРИМЕНЕНИЕ
Сверхчистый кремний преимущественно используется для производства одиночных электронных приборов (нелинейные пассивные элементы электрических схем) и однокристальных микросхем. Чистый кремний, отходы сверхчистого кремния, очищенный металлургический кремний в виде кристаллического кремния являются основным сырьевым материалом для солнечной энергетики.
Монокристаллический кремний — помимо электроники и солнечной энергетики, используется для изготовления зеркал газовых лазеров.
Соединения металлов с кремнием — силициды — являются широко употребляемыми в промышленности (например, электронной и атомной) материалами с широким спектром полезных химических, электрических и ядерных свойств (устойчивость к окислению, нейтронам и др.). Силициды ряда элементов являются важными термоэлектрическими материалами.
Соединения кремния служат основой для производства стекла и цемента. Производством стекла и цемента занимается силикатная промышленность. Она также выпускает силикатную керамику — кирпич, фарфор, фаянс и изделия из них. Широко известен силикатный клей, применяемый в строительстве как сиккатив, а в пиротехнике и в быту для склеивания бумаги. Получили широкое распространение силиконовые масла и силиконы — материалы на основе кремнийорганических соединений.
Технический кремний находит следующие применения:
- сырьё для металлургических производств: компонент сплава (бронзы, силумин);
- раскислитель (при выплавке чугуна и сталей);
- модификатор свойств металлов или легирующий элемент (например, добавка определённого количества кремния при производстве трансформаторных сталей уменьшает коэрцитивную силу готового продукта) и т. п.;
- сырьё для производства более чистого поликристаллического кремния и очищенного металлургического кремния (в литературе «umg-Si»);
- сырьё для производства кремний органических материалов, силанов;
- иногда кремний технической чистоты и его сплав с железом (ферросилиций) используется для производства водорода в полевых условиях;
- для производства солнечных батарей;
- антиблок (антиадгезивная добавка) в промышленности пластмасс.
Кремний (англ. Silicon) – Si
| Молекулярный вес | 28.09 г/моль |
| Происхождение названия | в переводе c др.-греч. κρημνός — «утёс, гора». |
| IMA статус | действителен |
Биологическое воздействие
Как и в литосфере, в организме человека кремний – один из топовых макроэлементов (до 4%).
О нехватке вещества сигнализирует следующие факторы:
- Тусклость, ломкость волос, ногтей.
- Сухость кожи.
- Частые ОРВИ, ОРЗ.
- Учащенное сердцебиение.
- Ослабленность скелета (позвоночные боли, остеопороз).
- Бесплодие.
Плюс пониженный иммунитет. У детей – замедление роста и общего развития.
Пополнить запас микроэлемента помогают продукты.
Больше всего вещества в продуктах, богатых клетчаткой:
- Необработанные крупы: рис, овес, ячмень, гречка.
- Все бобовые.
- Орехи, овощи, ягоды, фрукты,
В «животном» сегменте это мясо, яйца, морепродукты, молоко.
Риски
Чистый кремний — относительно инертное вещество, поэтому он обычно не накапливается в каком-либо органе или ткани, пока воздействие на него невелико. В виде порошка он может раздражать глаза, вызывая слезотечение или покраснение, при прикосновении к нему может возникнуть дискомфорт, зуд и шелушение.
При очень сильном воздействии кремний может повредить легкие; но без последствий, если количество не является достаточным, чтобы вызвать удушье. Однако это не относится к кварцу, который связан с раком легких и такими заболеваниями, как бронхит и эмфизема.
Кроме того, чистый кремний очень редко встречается в природе, а его соединения, которых так много в земной коре, не представляют опасности для окружающей среды.
Что касается кремнийорганического соединения, то они могут быть токсичными; но поскольку их много, это зависит от того, какой из них рассматривается, а также от других факторов (реактивность, pH, механизм действия и т. д.).
Структура и электронная конфигурация
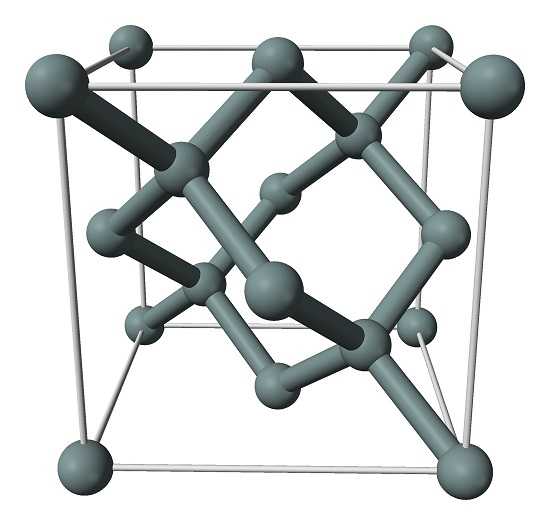
На изображении выше показана гранецентрированная кубическая структура (ГЦК), такая же, как у алмаза, для кристалла кремния. Серые сферы соответствуют атомам Si, которые, как видно, ковалентно связаны друг с другом; кроме того, они имеют тетраэдрическое окружение, воспроизводимое вдоль кристалла.
Кристалл кремния является ГЦК, потому что атом Si находится на каждой из граней куба (6 × 1/2). Точно так же есть восемь атомов Si в вершинах куба (8 × 1/8) и четыре, расположенных внутри него (те, которые показывают четко определенный тетраэдр вокруг них, 4 × 1).
При этом каждая элементарная ячейка содержит в общей сложности восемь атомов кремния (3 + 1 + 4, числа указаны в абзаце выше); характеристика, которая помогает объяснить его высокую твердость и жесткость, поскольку чистый кремний представляет собой ковалентный кристалл, подобный алмазу.
































